診療ガイドラインは、「健康に関する重要な課題について、医療利用者と提供者※1の意思決定を支援するために、システマティックレビューによりエビデンス総体※2を評価し、益と害のバランスを勘案して、最適と考えられる推奨を提示する文書」(Minds診療ガイドライン作成マニュアル編集委員会,2021)と定義されています。
診療ガイドラインを活用するには、診療ガイドラインの作成プロセス、エビデンスや推奨の強さ(推奨度)とは何か、ガイドラインの評価などについても知っておくことが大切です。このページでは、「Minds診療ガイドライン作成マニュアル」に沿って、診療ガイドラインの作成プロセスの大まかな流れを解説します。また、診療ガイドラインの評価ツールについても紹介します。
システマティックレビューやエビデンスに関する詳細は、以下をご覧ください。
診療ガイドラインの定義や診療ガイドライン作成マニュアルなどが掲載されています。
1.診療ガイドライン作成プロセス
診療ガイドラインの作成は、診療ガイドラインを作成する学会などの団体で、作成に携わる専門家の構成を検討し、組織を作るところから始まります。組織ができたら、診療ガイドラインの目的、取り扱う疾患や検査、治療などにおける重要なトピック(重要臨床課題)を検討し決定します。決定した重要臨床課題に基づいて、検査や治療方法など診療ガイドラインで答えるべきクリニカルクエスチョン(CQ)を設定します。CQを設定したら、システマティックレビューを行い、その根拠に基づいて、検査や治療方法などの推奨の強さ(推奨度)を決定し、診療ガイドラインとしてまとめます。
1)重要臨床課題の検討とクリニカルクエスチョン(CQ)の設定
クリニカルクエスチョン(CQ)とは、重要臨床課題の構成要素を抽出し、1つの疑問文で表現したものです。一般的に、構成要素を抽出する際には、PICOが用いられます。PICOとは、重要臨床課題の4つの構成要素の頭文字を取って略したものです。具体的な内容は以下の通りです。
- P(Patients、Problem、Population)
介入の対象となる患者の特性(性別や年齢など)
疾患や病態、症状など
特定の地理的条件や施設的要件など - I(Interventions)
Pに対して行うことを推奨するかどうか検討したい介入(検査や治療など)
介入の期間、薬の用量や投与方法などの要素 - C(Controls)
プラセボ(偽薬)、標準治療群など、比較する対照となる医療行為 - O(Outcomes)
介入(検査や治療など)が最も推奨されるか判断するための基準となるアウトカム(生存率、痛みや副作用、入院日数など患者に生じる結果)
PICOであげた構成要素を、「Pにおいて、Iを用いることが、Cと比較して、推奨されるか(例:早期の〇〇がんでは、内視鏡的切除と外科手術のどちらの方法が推奨されるか)」のような1つの文で表現したものがCQです。
診療ガイドラインの作成過程では多くのCQが作成されます。しかし、すべてのCQが診療ガイドラインに掲載されるわけではありません。中でも特に重要な、もしくは重大なアウトカムを扱うCQが採用されます。
2)研究論文の検索・収集(システマティックレビュー)と研究手法によるエビデンスの考え方
(1)システマティックレビュー
クリニカルクエスチョン(CQ)を決定したら、システマティックレビューを行います。システマティックレビューでは、設定したそれぞれのCQに関連する研究論文を文献データベースから系統的かつ網羅的に検索・収集します。収集した論文は、研究方法などの一定の基準で選択して評価し、複数の研究論文のエビデンス総体としてまとめます。
(2)研究手法によるエビデンスの考え方
エビデンスとは、あるテーマに関する試験や調査などの研究結果から導かれた、科学的な裏付けのことです。診療ガイドラインを作成する際には、収集した研究結果から得られたエビデンスが、どの程度信頼できるものなのかをよく検討する必要があります。
エビデンスがどの程度信頼できるものなのかについては、収集したそれぞれの研究手法によるエビデンスも含めて検討することが重要です。研究手法によるエビデンスの基準にはさまざまなものがありますが、例えば、米国臨床腫瘍学会(American society of clinical oncology: ASCO)の診療ガイドライン作成マニュアルには、研究手法別にピラミッド型の階層が示されています(図1)。
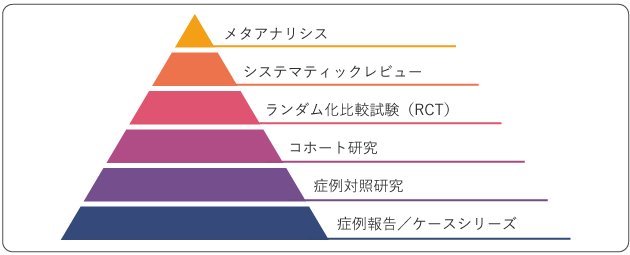
American Society of Clinical Oncology. ASCO Guidelines Methodology Manual, 2022年.より作成
システマティックレビュー:
設定したある疑問に関連する研究論文を過不足なく検索・収集し、類似した研究を一定の基準で選択・評価した上で、明確で科学的な手法を用いてまとめる研究
コホート研究:
ある要因の有無でグループを分け、追跡調査を行って疾病の発生などについて把握し、要因と疾病発症との関連を明らかにする研究方法
症例対照研究:
すでに疾病を発症しているグループとそうでないグループに分け、それぞれにおける過去の要因を比較することで、要因と疾病発症の関連を明らかにする研究方法
症例報告/ケースシリーズ:
1例または数例の患者に関する詳細な報告のこと
ASCOが作成する診療ガイドラインにおいては、エビデンスに基づく強い推奨を示すためには、ピラミッドの上位3層(メタアナリシス、システマティックレビュー、ランダム化比較試験)までのエビデンスのみを考慮するべきとされています。4層目以下の研究手法によるエビデンスを含める場合、その正当化には、説得力のある理論的根拠が求められ、推奨の程度はより弱く示されるべきとされています。
しかし、図1に表されているのは、研究手法によるエビデンスの一般的な傾向です。例えば、図1の最上位に位置しているメタアナリシスは、複数の研究を統合して統計解析を行う手法であるため、個々の研究の質や研究が行われた際の要素などにも影響を受けます。また、それぞれの研究の他の要素によっても、研究の結論が影響を受けることにも留意して、エビデンスを総合的に評価する姿勢が必要です。
3)エビデンスの確実性(強さ)と推奨の強さ(推奨度)の決定
(1)エビデンスの確実性(強さ)
エビデンスの確実性(強さ)とは、システマティックレビューによってまとめられたエビデンス総体が、検査や治療などの特定の医療行為を実施すること(あるいは実施しないこと)を推奨できるかどうかに関する確信の程度を示したものです。
多くの診療ガイドラインでは、クリニカルクエスチョン(CQ)ごとに、「エビデンス総体が、推奨を支持するものとしてどれほど適切か」がA~Dの4段階で示されています(表1)。エビデンスの確実性(強さ)は、推奨の強さ(推奨度)を決定する際の判定にも使われます。
| A(強) | 効果の推定値が推奨を支持する適切さに強く確信がある |
|---|---|
| B(中) | 効果の推定値が推奨を支持する適切さに中程度の確信がある |
| C(弱い) | 効果の推定値が推奨を支持する適切さに対する確信は限定的である |
| D(とても弱い) | 効果の推定値が推奨を支持する適切さにほとんど確信できない |
Minds診療ガイドライン作成マニュアル編集委員会.Minds診療ガイドライン作成マニュアル2020 ver. 3.0.公益財団法人日本医療機能評価機構EBM医療情報部.2021.より作成
(2)推奨の強さ(推奨度)
「推奨の強さ(推奨度)」は、検査や治療などの特定の医療行為を実施すること(あるいは実施しないこと)に関する推奨の程度です。クリニカルクエスチョン(CQ)に対する回答の形式で示されます。
推奨の強さ(推奨度)を決定する際には、システマティックレビューで示された、望ましい効果(益)と望ましくない効果(害や負担)のバランスや、エビデンスの確実性を中心に、患者の価値観や希望、費用対効果などの観点からも、多角的な検討が行われます。
推奨の強さ(推奨度)の付け方は診療ガイドラインによって異なりますが、通常は、「実施すること」と「実施しないこと」それぞれについて、「強く勧める」か「弱く勧める(条件付きで進める)」かの2種類の強さで示します(表2)。
ただし、すべての診療ガイドラインが表2の推奨の強さ(推奨度)を採用しているとは限りません。そのため、それぞれの診療ガイドラインの注意書きを読む必要があります。また、推奨の強さを「なし」として、明確な推奨ができないことが示されている場合もあります。
| 実施するかしないか | |||
|---|---|---|---|
| 実施することを勧める | 実施しないことを勧める | ||
| 推奨の強さ | 強い | 実施することを強く推奨する | 実施しないことを強く推奨する |
| 弱い (提案、条件付きの推奨など) |
実施することを弱く推奨する | 実施しないことを弱く推奨する | |
(公財)日本医療機能評価機構.Mindsガイドラインライブラリ.診療ガイドライン患者・市民向けQ&A;2022年.より作成
2.診療ガイドラインの評価
診療ガイドライン作成においては、そのプロセスを評価し、診療ガイドラインの質を担保することも重要です。診療ガイドラインの質を評価するための国際的なツールの1つに、AGREEⅡと呼ばれるものがあります。
AGREEⅡには、診療ガイドラインの作成において重要なポイントや、診療ガイドラインでどのような情報がどのように提供されるべきかなどが示されています。診療ガイドラインの活用にあたっては、AGREEⅡの項目(表3)もご確認ください。
AGREEⅡは、診療ガイドラインの対象や目的、作成の厳密さ、編集の独立性など6領域23項目について、7段階で評価します。
また、23項目の評価の過程で検討した基準を考慮し、診療ガイドラインの全体評価が行われます。全体評価では、診療ガイドラインの質を「1:低い」~「7:高い」の7段階で評価し、使用を推奨するかどうかを「推奨する」「推奨する(条件付き)」「推奨しない」で評価します。
| 領域1.対象と目的 |
| 1)ガイドライン全体の目的が具体的に記載されている。 |
| 2)ガイドラインが取り扱う健康上の問題が具体的に記載されている。 |
| 3)ガイドラインの適用が想定される対象集団(患者、一般市民など)が具体的に記載されている。 |
| 領域2.利害関係者の参加 |
| 4)ガイドライン作成グループには、関係するすべての専門家グループの代表者が加わっている。 |
| 5)対象集団(患者、一般市民など)の価値観や希望が調べられた。 |
| 6)対象となるガイドラインの利用者が明確に定義されている。 |
| 領域3.作成の厳密さ |
| 7)エビデンスを検索するために系統的な方法が用いられている。 |
| 8)エビデンスの選択基準が明確に記載されている。 |
| 9)エビデンス総体(body of evidence)の強さと限界が明確に記載されている。 |
| 10)推奨を作成する方法が明確に記載されている。 |
| 11)推奨の作成にあたって、健康上の益、副作用、リスクが考慮されている。 |
| 12)推奨とそれを支持するエビデンスとの対応関係が明確である。 |
| 13)ガイドラインの公表に先立って、専門家による外部評価がなされている。 |
| 14)ガイドラインの改訂手続きが示されている。 |
| 領域4.提示の明確さ |
| 15)推奨が具体的であり、曖昧でない。 |
| 16)患者の状態や健康上の問題に応じて、異なる選択肢が明確に示されている。 |
| 17)重要な推奨が容易に見つけられる。 |
| 領域5.適用可能性 |
| 18)ガイドラインの適用にあたっての促進要因と阻害要因が記載されている。 |
| 19)どのように推奨を適用するかについての助言・ツールを提供している。 |
| 20)推奨の適用に対する潜在的な資源の影響が考慮されている。 |
| 21)ガイドラインにモニタリングや監査のための基準が示されている。 |
| 領域6.編集の独立性 |
| 22)資金提供者の見解が、ガイドラインの内容に影響していない。 |
| 23)ガイドライン作成グループメンバーの利益相反が記録され、適切な対応がなされている。 |
(公財)日本医療機能評価機構.Mindsガイドラインライブラリ.AGREEⅡ 日本語訳(2022年9月改訂);2022年.より作成
3.引用文献・参考資料
- Minds診療ガイドライン作成マニュアル編集委員会.Minds診療ガイドライン作成マニュアル2020 ver. 3.0.公益財団法人日本医療機能評価機構EBM医療情報部.2021.
- (公財)日本医療機能評価機構.Mindsガイドラインライブラリ.診療ガイドライン患者・市民向けQ&A;2022年(閲覧日2023年6月28日)https://minds.jcqhc.or.jp/
- (公財)日本医療機能評価機構.Mindsガイドラインライブラリ.評価ツールAGREEⅡ;2022年(閲覧日2023年6月28日)https://minds.jcqhc.or.jp/
- American Society of Clinical Oncology. ASCO Guidelines Methodology Manual;2022年(閲覧日2023年6月28日)https://asco.org/
