急性リンパ性白血病(ALL)、急性骨髄性白血病(AML)の治療では、化学療法(細胞障害性抗がん薬を用いた治療)を基本的に行います。
1.急性リンパ性白血病(ALL)の治療
1)急性リンパ性白血病(ALL)の診断
白血病の診断は、骨髄中の白血病細胞の量と性質で決定されます。骨髄でリンパ芽球が全有核細胞数の25%以上まで増加し、顕微鏡で見た形態および特殊染色で急性リンパ性白血病由来のものと判定された場合に診断されます。また、白血病細胞の細胞表面マーカーによって、大きく前駆B細胞性、成熟B細胞性、T細胞性の3つに分けられており、治療方針を決めるための基準の1つとなります。
2)急性リンパ性白血病(ALL)の治療の選択
急性リンパ性白血病の治療の基本は、細胞障害性抗がん薬を用いた治療(化学療法)です(図3)。化学療法は数種類の薬剤を組み合わせた多剤併用療法で行い、寛解導入療法、強化療法、維持療法の3段階に分けて行います。
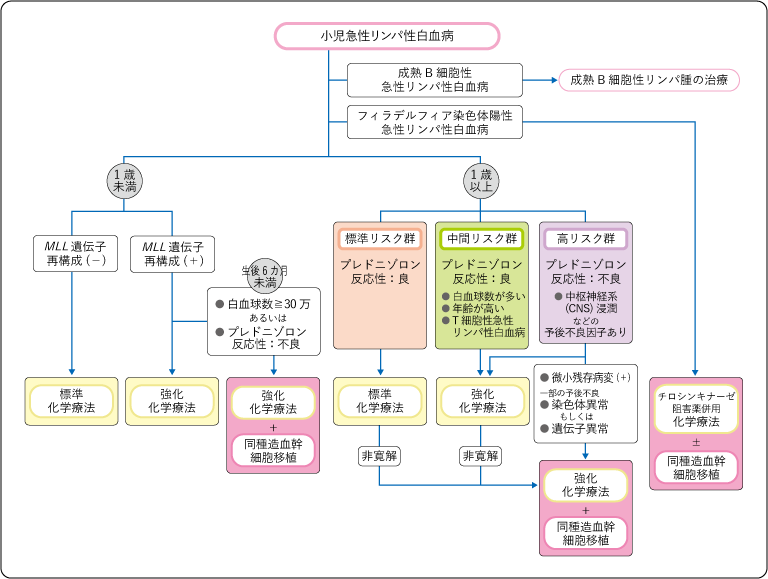
3)急性リンパ性白血病(ALL)の治療法
(1)寛解導入療法
白血病細胞の減少と症状の軽減を目的に行います。プレドニゾロン(またはデキサメタゾン)・ビンクリスチン・L-アスパラギナーゼ・アントラサイクリン系の4種類の薬剤を4~5週間かけて投与します。また、中枢神経系(脳と脊髄)への白血病細胞の浸潤を予防するため、メトトレキサートなどの薬剤を脳脊髄液(髄液)の中に注射します。
(2)強化療法
寛解導入療法の終了直後から、さらに白血病細胞を減少させることを目的に行います。早期強化療法では、寛解導入療法で使用していない薬剤を投与します。その後、寛解後強化療法として、寛解導入療法と早期強化療法を繰り返し行います。薬剤が届きにくい中枢神経系への浸潤予防として、メトトレキサートを含む薬剤の髄注療法や点滴による投与を行うこともあります。
(3)維持療法
強化療法に続いて、白血病細胞の根絶と再発予防を目的に行います。メルカプトプリンを連日、メトトレキサートを週1回と、2剤の内服が標準的な治療です。この時期は、学校生活などの通常の生活を送ることができます。維持療法も含め、最低2年間行うことが勧められています。
(4)造血幹細胞移植
初診時の染色体分析で、hypodiploid(低二倍体:通常は46本ある染色体数が44本以下)など予後の悪い染色体異常や遺伝子異常がある場合、または初期の治療反応が不良の場合には、通常の治療では再発のリスクが高いと考えられ、同種造血幹細胞移植が検討されます。
また、寛解導入療法開始後1カ月を経ても寛解にならない場合は、救援化学療法などを行い、寛解に到達できた時点で同種造血幹細胞移植が考慮されます。このほか、乳児急性リンパ性白血病で高リスクの場合や再発時に高リスクの場合など、化学療法のみで治療が難しい場合にも検討されます。
1)フィラデルフィア染色体陽性の場合
フィラデルフィア染色体が陽性の場合は、イマチニブなどの分子標的治療薬(病気の原因となっているタンパク質などの特定の分子にのみ作用するように設計された治療薬)と化学療法の併用を行います。寛解導入療法から維持療法終了までの期間、分子標的治療薬の服用を可能なかぎり継続することが重要です。
2)乳児の場合
1歳未満でKMT2A(MLLともいいます)という遺伝子の変化がある場合は、予後が不良な病型のため強力な多剤併用化学療法を行い、さらに高リスク群では同種造血幹細胞移植が検討されます。KMT2A遺伝子の変化がない場合は、通常の多剤併用化学療法を行います。
3)思春期・若年成人の場合
成人の治療法よりも小児の治療法の方が治療成績は良好です。そのため小児の治療法と同じように、寛解導入療法、強化療法、維持療法の3段階に分かれた多剤併用化学療法を行います。
4)急性リンパ性白血病(ALL)の予後因子
これまでの治療成績より、治療効果に影響するさまざまな要因が明らかになっています。これらを予後因子と呼びます。年齢や初診時の白血球数、白血病細胞の染色体・遺伝子異常、免疫学的分類、初期治療の反応性、中枢神経系への浸潤の有無などによって治療効果が異なります。
2.急性骨髄性白血病(AML)の治療
1)急性骨髄性白血病(AML)の診断
治療方針を決定する上で重要となる分類は病型分類と呼ばれます。治療成績の蓄積や比較のために統一した分類で診断することが重要となるため、国際的にWHO分類(表1)が用いられています。
| 1) | 特異的染色体異常を有する急性骨髄性白血病 | |
|---|---|---|
| (a) | t(8;21) (q22;q22.1)、RUNX1-RUNX1T1を有する急性骨髄性白血病 | |
| (b) | inv(16) (p13.1q22)またはt(16;16) (p13.1;q22)、CBFB-MYH11を有する急性骨髄性白血病 | |
| (c) | PML-RARAを有する急性前骨髄球性白血病 | |
| (d) | t(9;11) (p21.3;q23.3)、MLLT3-KMT2Aを有する急性骨髄性白血病 | |
| (e) | t(6;9) (p23;q34.1)、DEK-NUP214を有する急性骨髄性白血病 | |
| (f) | inv(3) (q21.3q26.2) またはt(3;3) (q21.3;q26.2)、GATA2、MECOMを有する急性骨髄性白血病 | |
| (g) | t(1;22) (p13.3;q13.3)、RBM15-MKL1を有する急性骨髄性白血病(巨核芽球性) | |
| (h) | 暫定分類:BCR-ABL1遺伝子変異を有する急性骨髄性白血病 | |
| (i) | NPM1遺伝子変異を有する急性骨髄性白血病 | |
| (j) | 両アレルのCEBPA遺伝子変異を有する急性骨髄性白血病 | |
| (k) | 暫定分類:RUNX1遺伝子変異を有する急性骨髄性白血病 | |
| 2) | 骨髄異形成関連の変化を有する急性骨髄性白血病 | |
| 3) | 治療に関連した急性骨髄性白血病と骨髄異形成症候群 | |
| 4) | 上記以外の急性骨髄性白血病 | |
| (a) | 急性骨髄性白血病最未分化型 | |
| (b) | 急性骨髄性白血病未分化型 | |
| (c) | 急性骨髄性白血病分化型 | |
| (d) | 急性骨髄単球性白血病 | |
| (e) | 急性単球性白血病および急性単芽球性白血病 | |
| (f) | 純赤芽球性白血病 | |
| (g) | 急性巨核芽球性白血病 | |
| (h) | 急性好塩基球性白血病 | |
| (i) | 骨髄線維症を伴う急性汎骨髄症 | |
| 5) | 骨髄肉腫 | |
| 6) | ダウン症候群に関連した骨髄増殖症 | |
| (a) | 一過性骨髄異常増殖症(TAM) | |
| (b) | ダウン症候群関連骨髄性白血病 | |
*染色体異常の記号の説明
|
||
Swerdlow SH, editors. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. 2017, IARC. より作成
大きくは、①ダウン症候群に合併した急性骨髄性白血病、②急性前骨髄球性白血病、③それ以外の急性骨髄性白血病の3つの病型に分かれており、それぞれ異なった治療が行われます(図4)。
2)急性骨髄性白血病(AML)の治療の選択
急性骨髄性白血病の治療の基本は、細胞障害性抗がん薬を用いた治療(化学療法)です(図4)。化学療法は、数種類の薬剤を組み合わせた多剤併用療法で行い、寛解導入療法と強化療法に分けて行います。予後因子に基づいて低リスク群・中間リスク群・高リスク群に分類され、それぞれに適した強さの治療を行います。
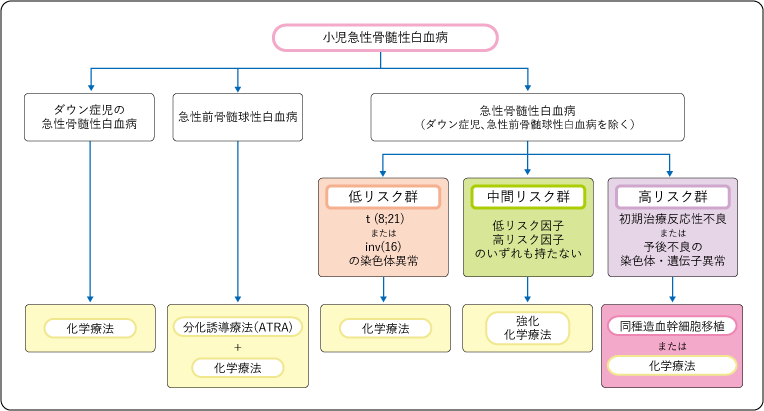
3)急性骨髄性白血病(AML)の治療法
(1)寛解導入療法
白血病細胞の減少と症状の軽減を目的に行います。アントラサイクリン系の薬剤を3~5日間とシタラビンを7~10日間投与します。また、この2剤にエトポシドを併用する場合もあります。
(2)強化療法
寛解導入療法の終了直後から、さらに白血病細胞を減少させることを目的に行います。アントラサイクリン系の薬剤と大量シタラビン療法を含んだ多剤併用化学療法を行います。寛解導入療法と併せて5~6コース行います。通常、急性リンパ性白血病と異なり維持療法は行いません。
(3)造血幹細胞移植
初診時の染色体・遺伝子異常で、予後が不良な型であった場合や、初期治療の反応性から再発のリスクが高いとされる高リスク群に対しては、寛解が得られた時点で同種造血幹細胞移植が検討されます。
移植のドナーはHLA(白血球の型)が一致するきょうだいの骨髄が第一選択ですが、ドナーがみつからない場合はHLAが一致する非血縁骨髄移植や、非血縁臍帯血移植を行います。これらの治療でも良好な成績が得られています。
1)急性前骨髄球性白血病(APL)の場合
急性前骨髄球性白血病のほとんどで、t(15;17)という染色体異常がみつかります。播種性血管内凝固症候群という重篤な合併症を伴うことがあるため、診断後すぐに治療を開始することが重要です。
寛解導入療法は、全トランスレチノイン酸(ATRA)とアントラサイクリン系の薬剤にシタラビンを加えた多剤併用化学療法です。完全寛解に到達した後は、ATRAとアントラサイクリン系の薬剤を中心とした複数回の強化療法、ATRAによる維持療法を行います。
最近は、ATRAと、ATRAと類似の効果をもつ三酸化ヒ素(ATO)を組み合わせた治療を行うことも多くなってきています。
2)ダウン症候群の患者にAMLが発症した場合
ダウン症候群の患者に発症したAMLは、4歳以下での発症や急性巨核芽球性白血病が多いなどの特徴があります。治療による合併症が起こりやすい一方で治療の反応性は良いことから、アントラサイクリン系の薬剤とシタラビンを中心とした、通常の急性骨髄性白血病の治療より強度を弱めた多剤併用化学療法を行います。
3.緩和ケア/支持療法
1)緩和ケアについて
痛みには身体的な痛みと精神的な痛みがありますが、両方が入り混じって、どちらとも区別できない場合もあります。医療者と家族は子どもが訴える痛みを受け止め、よく話し合って対処することが大切です。
最近は新しい鎮痛薬が次々に開発され、身体的痛みはうまくコントロールされるようになってきました。飲み薬や点滴注射のほか、貼り薬や坐薬などもあります。細胞障害性抗がん薬を上手に使うことで、痛みがやわらぐことももちろんあります。モルヒネなどの医療用麻薬はあまり使いたくないという人もいますが、適当な時期に適切に使えば決して怖い薬ではありません。
2)支持療法について
支持療法とは、がんそのものによる症状やがんの治療に伴う副作用・合併症・後遺症を軽くするための予防、治療およびケアのことを指します。
細胞障害性抗がん薬を使うと、血液をつくる力が一時的に抑制されます(骨髄抑制)。その回復を待つ間、赤血球や血小板の減少に対しては輸血を行って対処します。また、白血球が減少している間は免疫力が低下しているため、外泊はできません。熱が出た場合はたとえ元気であっても重篤な感染症になってしまう可能性があるため、抗菌薬(抗生物質)を早めに使うことになります。また、免疫力の低下している状態が長く続くと「ニューモシスチス肺炎(カリニ肺炎)」という肺炎になってしまうことがあり、予防するために「ST合剤(バクタ、ダイフェン)」を飲むこともあります。また、細胞障害性抗がん薬は吐き気を引き起こすことがあるため、吐き気止めを使って症状の緩和を手助けします。
4.再発
再発とは、治療によって検査上がんが認められなくなった後、再びがんが出現することをいいます。治療後は、定期的に通院して経過をみることが大切です。
1)急性リンパ性白血病(ALL)の再発時の治療
再発時期、部位、白血病細胞の免疫学的分類に基づいて、リスク分類(低リスク・中間リスク・高リスク群)し、それぞれに応じた治療を行います。
初発時と同様に多剤併用の化学療法が基本です。中間リスク群では、寛解導入療法後に寛解かつ微小残存病変(MRD)が陰性化した場合は化学療法を継続します。中間リスク群で寛解導入療法後のMRDが残存する場合や、高リスク群の場合は、救援化学療法などで寛解に到達できた時点で同種造血幹細胞移植が検討されます。ブリナツモマブやイノツズマブ・オゾガマイシンといった抗体薬が使用されることもあります。また、再発後に寛解が得られない場合や、造血幹細胞移植後の再発の場合は、キメラ抗原受容体遺伝子改変T細胞療法(CAR-T)が行われることがあります。
低リスク群は、中枢神経や精巣などの骨髄外のみの晩期再発である場合に該当します。中枢神経再発では、多剤併用化学療法と髄注による中枢神経治療の後、局所放射線照射と維持療法を行います。精巣単独再発では、局所治療(放射線治療や手術)と多剤併用化学療法を行います。
2)急性骨髄性白血病(AML)の再発時の治療
多くの場合は骨髄中のみの再発です。初発時と同様、アントラサイクリン系の薬剤とシタラビンなどを組み合わせた寛解導入療法が行われます。寛解が得られた時点で、同種造血幹細胞移植を行うことが勧められます。
| 2022年06月06日 | 構成を変更し、内容を更新しました。 |
| 2021年11月08日 | 関連情報に「小児白血病・リンパ腫の診療ガイドライン 第1章急性リンパ性白血病 ALL」「小児白血病・リンパ腫の診療ガイドライン 第2章急性骨髄性白血病 AML」を追加しました。 |
| 2018年03月07日 | 4タブ形式に変更し、「臨床試験」の項目を追加しました。 |
| 2017年02月01日 | 「小児白血病・リンパ腫診療ガイドライン 2016年版」「造血器腫瘍取扱い規約 2010年3月(第1版)」より内容を更新しました。 |
| 2016年07月08日 | 特殊なタイプに対しての治療「PL」を「APL」に修正しました。 |
| 2014年04月22日 | 2013年6月発行の冊子とがん情報サービスの情報を再編集し、掲載しました。 |
