胃がんの治療には、内視鏡治療、手術(外科治療)、薬物療法(化学療法)などがあります。
また、診断されたときから、がんに伴う心と体のつらさなどを和らげるための緩和ケア/支持療法を受けることができます。つらいときは遠慮せずに医療者やがん相談支援センターに相談しましょう。
1.ステージと治療の選択
治療は、がんの進行の程度を示すステージ(病期)やがんの性質、体の状態などに基づいて検討します。胃がんの治療を選択する際には、次のことを調べます。
1)ステージ(病期)
がんの進行の程度は、「ステージ(病期)」として分類します。ステージは、ローマ数字を使って表記することが一般的で、Ⅰ期(ステージ1)・Ⅱ期(ステージ2)・Ⅲ期(ステージ3)・Ⅳ期(ステージ4)と進むにつれて、より進行したがんであることを示しています。なお、胃がんではステージのことを進行度ということもあります。
胃がんのステージは、Ⅰ期~Ⅳ期まであり、次のTNMの3種のカテゴリー(TNM分類)の組み合わせで決まります。
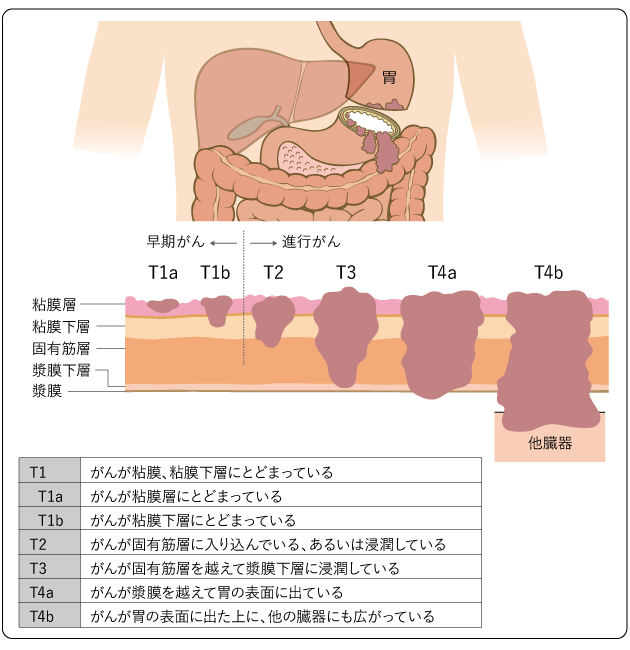
Tカテゴリー:原発巣※の深達度(がんの深さ)(図4)
Nカテゴリー:領域リンパ節(原発巣の近くにあるリンパ節)への転移の有無
Mカテゴリー:遠隔転移(がんができた場所から離れた臓器やリンパ節への転移)の有無
※原発巣とは、原発部位(がんが初めに発生した部位)にあるがんのことです。
胃がんでは、がんの深達度が粘膜および粘膜下組織にとどまるT1のものを「早期胃がん」といい、粘膜下組織を越えて広がるものを「進行胃がん」といいます。
なお、胃がんの治療方針を決めるためのステージ(病期)には、臨床分類と病理分類の2つの分類があります。
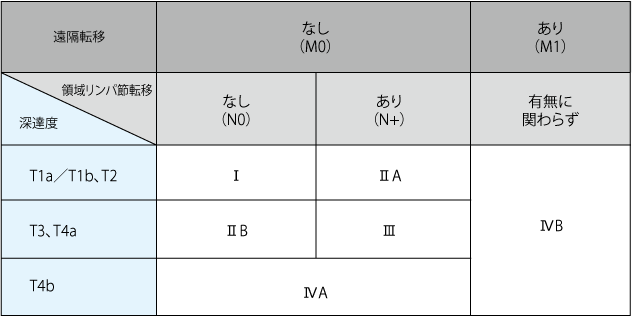
(1)臨床分類
臨床分類は、治療方針を決めるときに使う分類です。画像診断や生検、審査腹腔鏡などの結果に基づいてがんの広がりを推定します(表1)。
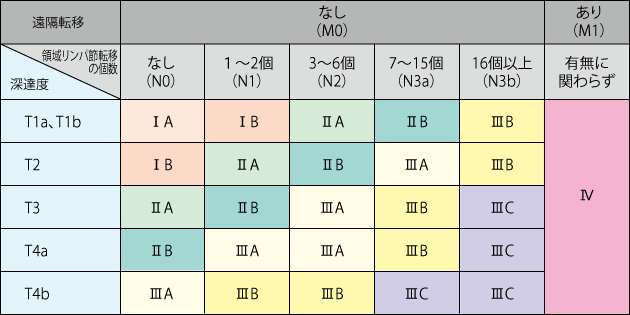
(2)病理分類
病理分類は、手術で切除した病変を病理診断し、実際のがんの広がりを評価した分類です。術後補助化学療法が必要かどうかなど、手術後の治療方針を判断したりするときなどにも使われます(表2)。病理分類による分類は、手術前の検査によって推定した臨床分類と一致しない場合があり、術後にステージが変わることもがあります。
2)治療の選択
治療は、がんの進行度(ステージ)に応じた標準治療を基本として、本人の希望や生活環境、年齢を含めた体の状態などを総合的に検討し、担当医と話し合って決めていきます。
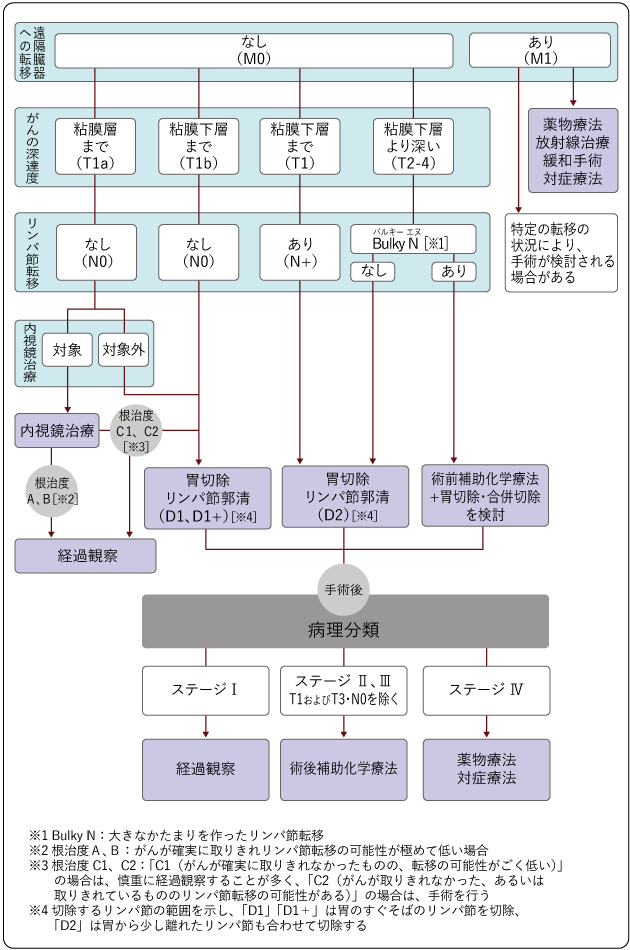
図5は、胃がんの標準治療を示したものです。担当医と治療方針について話し合うときの参考にしてください。
遠隔臓器(胃以外の臓器)やリンパ節への転移がなく、がんの深達度が粘膜までにとどまる場合は、内視鏡治療(内視鏡的切除)が中心です。がんが粘膜下組織に達しているときは、手術(外科治療)を検討します。手術後には、切除した病変の病理分類を行い、必要に応じて薬物療法が行われることがあります。遠隔臓器への転移がある場合には、状況によって、薬物療法などの治療法を検討します。
なお、内視鏡治療の対象になるかどうかに関する詳細は、次の「2.内視鏡治療(内視鏡的切除) 1)内視鏡治療の方法」をご覧ください。
妊孕性の温存について
がんの治療が、性別にかかわらず妊孕性(子どもをつくる力)に影響することがあります。将来子どもをもつことを希望している場合には、妊孕性を温存することが可能かどうかを、治療開始前に担当医に相談してみましょう。
禁煙について
喫煙を続けることは、がんの治療の効果を下げる原因になると考えられています。喫煙している場合には、治療が始まる前に少しでも早く禁煙しましょう。なお、手術までに禁煙できていない時には、延期されることもあります。禁煙治療を希望する場合は、まずはがんの治療の担当医に相談しましょう。
2.内視鏡治療(内視鏡的切除)
内視鏡を使って胃の内側からがんを切除する方法で、がんが粘膜にとどまっている場合に行われます。リンパ節転移の可能性がごく低い早期のがんで、一度に切除できると考えられる場合に行うのが原則です。手術と比べると、体に対する負担が少なく、がんの切除後も胃が残るため、食生活への影響が少ない治療法です。
内視鏡治療でがんが確実に取りきれたかどうかは、病理診断で確認します。がんが確実に取りきれ、リンパ節転移の可能性が極めて低い場合(根治度A、B)には、経過を観察します。がんが確実に取りきれなかったものの、転移の可能性がごく低い場合(根治度C1)には、再度内視鏡による治療が行われたり、慎重に経過を観察するなどします。一方、がんが内視鏡治療では取りきれなかった、あるいは取りきれているが、深さが粘膜下組織まで達しているなどの理由でリンパ節転移の可能性がある場合(根治度C2)は、後日、追加で手術が必要となります(前項の「1.ステージと治療の選択 2)治療の選択」図5をご覧ください)。
1)内視鏡治療の方法
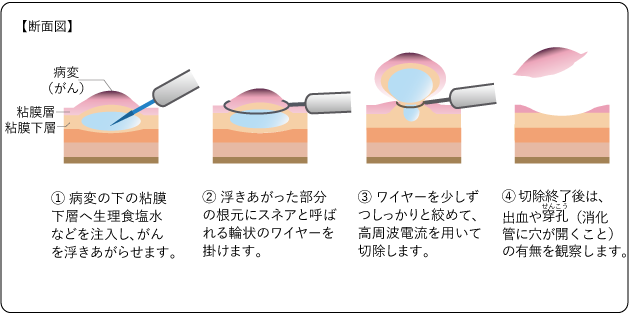
内視鏡の先端から、スネアと呼ばれる輪状の細いワイヤーをかけて、病変を切除する内視鏡的粘膜切除術(EMR)(図6)、高周波ナイフで粘膜下組織から病変をはぎ取るように切除する内視鏡的粘膜下層剥離術(ESD)(図7)があります。
EMRはがんの大きさが2cm以下で潰瘍のないことが条件です。ESDは、より大きながんの場合や、潰瘍があっても行えることがあります。
2)内視鏡治療の合併症
治療後に、出血や胃に穴が開く穿孔が起こることがあります。出血や穿孔が起こると、吐き気や嘔吐、吐血や下血、腹痛などの症状が出てきます。その他にも、発熱やめまいなど、治療後に何らかの体調の変化を感じたときには、医師や看護師に伝えることが必要です。
3.手術(外科治療)
遠隔転移がなく、内視鏡治療による切除が難しい場合には、手術による治療が推奨されています。
手術には、おなかを20cmほど切開する開腹手術と、おなかに小さい穴を開けてそこから専用の器具を挿入して手術を行う腹腔鏡下手術やロボット支援手術があります。
腹腔鏡下手術やロボット支援手術が推奨されるかどうかは、がんの進行度などによって異なります。また、十分な知識や経験をもつ医師が行うことなどの条件があり、実施できる施設は限られています。この手術が可能かどうかは、担当医とよく相談してください。
なお、胃がんの手術では、胃を切除した後にさまざまな後遺症が起こる可能性があります。そのため、特に高齢である場合などは、年齢だけでなく心臓や肺、肝臓、腎臓などの機能が十分であるか、手術後の生活や必要なサポートが受けられるかどうかということも重要な要素です。
入院期間は、手術の大きさや体の状態、他に病気があるかどうかによりますが、一般的には手術前1~2日程度、手術後7~14日程度です。
1)手術の方法
手術では、がんと胃の一部またはすべてを取り除きます。同時に胃の周囲のリンパ節を取り除くリンパ節郭清や、食べ物の通り道をつくり直す再建手術(消化管再建)も行われます。
(1)胃の切除範囲
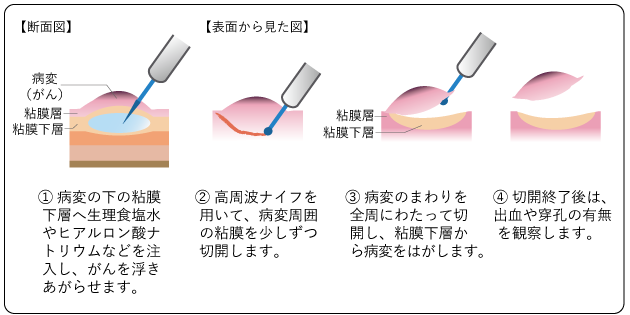
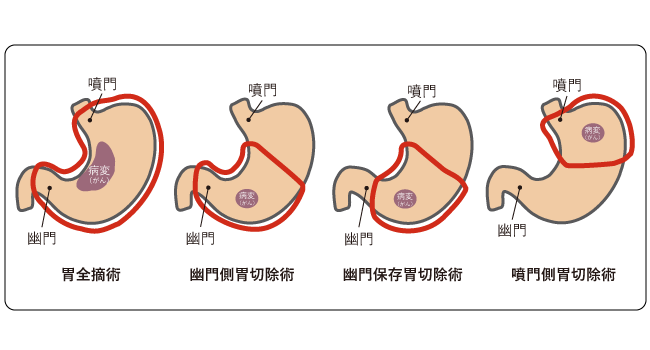
切除する胃の範囲は、がんのある部位と進行度によって決まります。胃の切除範囲によっていくつかの方法があり、代表的なものは、胃全摘術、胃亜全摘術、幽門側胃切除術、幽門保存胃切除術、噴門側胃切除術です(図8)。
(2)リンパ節郭清
胃を切除する際に、胃の周囲にあるリンパ節も切除します。これをリンパ節郭清といいます。胃のすぐそばのリンパ節と、胃から少し離れたリンパ節を合わせて切除する「D2リンパ節郭清」が標準的に行われます。早期がんで、リンパ節転移の可能性が低い場合には、郭清するリンパ節の範囲を狭くした「D1リンパ節郭清」または「D1+リンパ節郭清」が行われます(前項の「1.ステージと治療の選択 2)治療の選択」図5をご覧ください)。
(3)消化管再建
消化管再建とは、胃の切除手術の際に、食道と残った胃や腸などの消化管を縫い合わせてつなぎ、新しく食べ物の通り道を造り直すことです。再建の方法にはいくつかの種類があり、胃の切除範囲などによって決まります。
(4)周辺臓器の合併切除
胃の周囲にある、肝臓、横隔膜、膵臓、胆のう、十二指腸、横行結腸などの臓器にがんが浸潤している場合、胃の切除と同時に、これらの臓器の一部を切除することがあります。これを他臓器合併切除といい、がんを完全に切除することを目指して行われます。
2)手術の合併症
胃がんの手術に伴う主な合併症として、縫合不全や膵液漏、これらに伴う腹腔内膿瘍などがあります。
(1)縫合不全
手術のときに消化管を縫い合わせたところがうまくつながらず、つなぎ目から食べ物や消化液が漏れることを縫合不全といいます。縫合不全になると炎症が起こり、痛みや熱が出るのが特徴です。悪化した場合、腹膜炎が起こり、再手術が必要になる場合があります。
(2)膵液漏
膵臓の周りのリンパ節郭清を行ったときに、一時的に膵液が漏れ出すことを膵液漏といいます。膵液は、タンパク質や脂肪を分解する酵素を含むので、膵液漏が起こると、周囲の臓器や血管を溶かし、感染が起こって膿瘍(膿がたまること)ができたり、出血を起こしたりすることがあります。
(3)腹腔内膿瘍
縫合不全や膵液漏によって感染が起こり、おなかの中にできた膿のかたまりを腹腔内膿瘍といいます。膿瘍ができる場所により症状は異なりますが、多くの場合、腹痛や発熱といった症状があらわれます。画像検査で確認し、膿瘍ができていれば、感染を抑えるために抗菌薬を使います。また、膿を外に出すためのカテーテルを体の中に一定期間入れておく場合もあります。
(4)その他、手術後に起こる症状と食事の注意点
胃を切除したあとは、食後に動悸、発汗、めまいなどが起こるダンピング症候群や、貧血などにもなりやすくなるため、食事のとり方や内容にも注意が必要です。詳細は、関連情報「胃がん 療養 2.日常生活を送る上で 2)手術(外科治療)後に起こる症状と食事の注意点」をご覧ください。
4.薬物療法(化学療法)
胃がんの薬物療法には、大きく分けて「手術によりがんを取りきることが難しい進行・再発胃がんに対する化学療法」と、手術後の再発予防を目的とする「術後補助化学療法」があります。なお、リンパ節への転移がある場合や、手術で取りきることが難しい場合は、手術の前に「術前補助化学療法」が行われる場合もあります。胃がんの薬物療法で使う薬には、細胞障害性抗がん薬、分子標的薬、免疫チェックポイント阻害薬があります。治療は、これらの薬を単独または組み合わせて、点滴もしくは内服で行います。
細胞障害性抗がん薬は、細胞が増殖する仕組みの一部を邪魔することで、がん細胞を攻撃する薬です。分子標的薬は、がん細胞の増殖に関わるタンパク質などを標的にして、がんを攻撃する薬です。免疫チェックポイント阻害薬は、免疫ががん細胞を攻撃する力を保つ(がん細胞が免疫にブレーキをかけるのを防ぐ)薬です。
薬物療法の効果は、内視鏡検査やCT検査で確認します。また、転移した臓器に対する治療の効果は主にCT検査で確認します。このほかに、MRI検査やPET検査などで確認することもあります。
1)手術によりがんを取りきることが難しい進行・再発胃がんに対する薬物療法
遠隔転移がある場合など、手術でがんを取りきることが難しい場合や、がんが再発した場合に行われます。薬物療法だけでがんを完全に治すことは難しいですが、がんの進行を抑えたり、がんによる症状を和らげたりすることが分かっています。薬物療法を受けられるかどうかは、以下の条件などを参考に検討します。
- 病理診断が行われ、病理分類が確認されている
- 体の状態を表す指標の1つであるパフォーマンスステータスが良好(0から2)である
- 心臓、肝臓、肺などの主な臓器の機能が保たれている
- 他に重い病気がない
治療には、一次化学療法から四次化学療法以降までの段階があります(図9)。
一次化学療法の前には、以下のバイオマーカー検査を行い、その結果に基づいて、薬剤を選択することが勧められています。
- HER2検査:HER2はがん細胞の増殖を促すタンパク質です。HER2を過剰に作っているがん細胞がどの程度あるかを調べ、一定以上の場合にHER2陽性と判定します。胃がんの人の約15~20%にHER2が過剰に現れていると言われています。
- PD-L1検査:PD-L1というタンパク質があるがん細胞の割合を調べます。PD-L1がどれくらい現れているかはCPS(Combined Positive Score)で示します。
- CLDN18検査:CLDN18というタンパク質が現れているがん細胞がどれくらいあるかを調べます。
- MSI検査:MSI-High(遺伝子に入った傷を修復する機能が働きにくい状態)でないかどうかを調べます。胃がんの人の約5%はMSI-Highの状態と言われています。
これらの検査結果に基づき、まずは一次化学療法から始め、治療の効果が低下した場合や、副作用が強く治療を続けることが難しい場合には二次化学療法、三次化学療法、四次化学療法以降と治療を続けていきます。
(1)一次化学療法
一次化学療法で使う薬剤は、がんの組織におけるHER2およびCLDN18の状態によって決まります。
HER2陽性の場合は、細胞障害性抗がん薬とHER2に対する分子標的薬、およびPD-L1検査の結果によっては免疫チェックポイント阻害薬を組み合わせて治療します。
HER2陰性でCLDN18が陽性の場合は、細胞障害性抗がん薬とCLDN18に対する分子標的薬、または細胞障害性抗がん薬と免疫チェックポイント阻害薬を組み合わせて治療します。なお、免疫チェックポイント阻害薬を使うかどうかは、PD-L1検査やMSI検査の結果から検討します。
HER2陰性でCLDN18が陰性の場合は、細胞障害性抗がん薬と免疫チェックポイント阻害薬を組み合わせて治療します。
(2)二次化学療法
二次化学療法では、一次化学療法で使用しなかった細胞障害性抗がん薬と分子標的薬を組み合わせて用います。組み合わせた治療が難しい場合は、細胞障害性抗がん薬を1種類のみ使うこともあります。
MSI-Highで、一次化学療法で免疫チェックポイント阻害薬を使用しなかった場合には、免疫チェックポイント阻害薬を用いることがあります。
(3)三次化学療法
三次化学療法では、HER2陰性の場合には、二次化学療法までに使用しなかった細胞障害性抗がん薬、もしくは免疫チェックポイント阻害薬のいずれかを用います。なお、二次化学療法までに免疫チェックポイント阻害薬を使用した場合は、三次化学療法で用いることは推奨されていません。
HER2陽性の場合は、一次化学療法、二次化学療法とは異なる種類の分子標的薬(抗体薬物複合体)を用います。胃がん治療で使用する抗体薬物複合体は、HER2を標的にした抗体に細胞障害性抗がん薬を組み合わせた薬剤です。
(4)四次化学療法以降
四次化学療法以降は、三次化学療法までで候補になった薬のうち、使用しなかった薬剤に切り替えて治療することを検討します。
2)術後補助化学療法
手術でがんを切除できても、目に見えないようなごく小さながんが残っていて、後に再発することがあります。こうした小さながんによる再発を予防する目的で行われる化学療法を術後補助化学療法といい、手術後の病理分類で、ステージがⅡまたはⅢの場合に行うことが推奨されています。
手術後の体の状態やがんの進行度によって、細胞障害性抗がん薬の内服か、細胞障害性抗がん薬の内服と他の種類の細胞障害性抗がん薬の点滴を併用する方法を検討します。治療の期間は、1種類の細胞障害性抗がん薬を内服する場合は1年間、他の薬と併用する場合は薬の種類によって異なりますが、6カ月もしくは1年間続けることが推奨されています。
3)薬物療法の副作用について
薬の種類や個人によって、副作用の症状や程度、副作用が起こる時期には違いがあります。
細胞障害性抗がん薬の副作用には、口内炎、吐き気、脱毛、下痢など自分で分かるものと、血液中の白血球や血小板などの数が少なくなって感染や出血が起こりやすくなる骨髄抑制、肝機能や腎機能の悪化など検査で分かるものがあります。分子標的薬や免疫チェックポイント阻害薬の副作用は、薬の種類ごとにさまざまです。
最近では副作用を予防する薬なども開発され、特に吐き気や嘔吐については、以前と比べてかなり抑えることができるようになってきました。
一方で、副作用の種類や程度によっては、治療を延期したり、薬の投与量を減らしたりすることもあります。副作用がある中で治療を続けると、症状が悪化したり、回復までに時間がかかったり、治療が継続できなくなることもあるためです。
治療が始まる前に、自分が受ける薬物療法はいつどんな副作用が起こりやすいか、どう対応したらよいか、特に気を付けるべき症状は何かなど、担当医や薬剤師、看護師によく確認しておくことも大切です。副作用と思われる症状があるときは、我慢せずに医療者に伝えましょう。副作用が起こった時に使用できる薬もいくつか選択肢があります。どのように対処していくか、医療者と一緒に考えていきましょう。
5.免疫療法
免疫療法は、免疫の力を利用してがんを攻撃する治療法です。2025年12月現在、胃がんの治療に効果があると証明されている免疫療法は、免疫チェックポイント阻害薬を使う方法のみです。手術でがんを取りきることが難しい進行・再発胃がんの場合に用いられることがあります。詳しくは、「4.薬物療法(化学療法)」をご覧ください。
6.緩和ケア/支持療法
緩和ケア/支持療法は、がんに伴う体と心のつらさ、社会的なつらさを和らげたり、がんそのものによる症状やがんの治療に伴う副作用、合併症、後遺症を軽くしたりするために行われる予防、治療およびケアのことです。がんと診断された時から、治療とともにつらさを感じるときにはいつでも受けることができます。痛みなどの症状がある場合には薬の処方など、気持ちの落ち込みやつらさには心理的なケアなどを受けることができます。治療中の副作用の予防や軽減のためのケアも含まれます。
胃がんが進行した場合は、消化管が狭くなることによる吐き気や嘔吐、腹水がたまることによるおなかの張りや痛み、だるさや倦怠感などの症状があらわれることもあります。胃の出口がふさがっている場合は、食事ができるように別の通り道をつくるバイパス術や、ステントと呼ばれるチューブのような器具を入れる治療が勧められることもあります。
このような症状や、本人にしか分からないつらさについても、遠慮せずに、早めに医療者やがん相談支援センターに相談することが大切です。緩和ケアは、全国のがん診療連携拠点病院で外来・入院いずれの状況でも受けることができ、自宅でも受けることができます。必要時には地域の病院と連携して緩和ケアを継続することも可能です。がん相談支援センターでは、お住まいの地域の病院や在宅療養、利用できる制度など地域の緩和ケアに関する情報を紹介することもできます。
また、がんやがんの治療によって外見が変化することがあります。支持療法の中でも、外見の変化によって起こるさまざまな苦痛を軽減するための支援として行われているのが、「アピアランス(外見)ケア」です。外見が変化することによる悩みや心配についても、医療者やがん相談支援センターに相談してみましょう。
7.リハビリテーション
リハビリテーションは、がんやがんの治療の体への影響に対する回復力を高め、今ある体の能力を維持、向上させるために行います。また、緩和ケアの一環として、心や体のさまざまなつらさを和らげる目的でも行います。
一般的に、治療中や治療後は体を動かす機会が減り、身体機能が低下します。そこで、医師の指示の下、筋力トレーニングや有酸素運動、日常の身体活動などをリハビリテーションとして行うことが大切だと考えられています。まずは無理のないように、散歩などの軽い運動から始めることが勧められています。体調を見ながら少しずつ歩く距離を増やすとよいでしょう。胃がんの手術後は、体重が減少する場合があり、それだけで立ちくらみなどが起きやすくなります。日常生活の中でできるトレーニングについては、医師や看護師などの医療者に確認しましょう。
8.再発した場合の治療
再発とは、治療によって見かけ上なくなったことが確認されたがんが、再び現れることです。原発巣のあった場所やその近くに、がんが再びあらわれることだけでなく、別の臓器で「転移」として見つかることも含めて再発といいます。
胃がんの場合は、初回の内視鏡治療あるいは手術(外科手術)で、目で見える範囲のがんをすべて取り除いたあとや、術後補助化学療法のあとに、治療した場所または離れた別の臓器やリンパ節に再びがんが見つかることをいいます。胃がんの転移には、主に肝臓や肺などに転移する血行性転移、リンパ行性転移、腹膜播種があります。
再発した場合の治療は、再発した部位、体の状態や前回の治療法とそのときの効果などにより決まります。薬物療法(化学療法)による治療が一般的です。
| 2026年01月13日 | 「胃癌治療ガイドライン医師用 2025年3月改訂【第7版】」「患者さんのための胃がん治療ガイドライン 2023年版」より、内容を更新しました。 |
| 2022年07月26日 | 「胃癌治療ガイドライン医師用 2021年7月改訂【第6版】」より、内容を更新しました。 |
| 2019年04月08日 | 「胃癌治療ガイドライン医師用 2018年1月改訂(第5版)」「胃癌取扱い規約 第15版(2017年10月)」により、内容を全面的に更新をするとともに、4タブ形式に変更しました。 |
| 2016年02月10日 | 「2.治療成績」の5年相対生存率データを更新しました。 |
| 2015年10月31日 | 「胃癌治療ガイドライン 2014年第4版」などにより、「4.化学療法」などを更新しました。 |
| 2015年10月31日 | 最新の情報を確認し、「3.自分にあった治療法を考える」などを更新しました。 |
| 2015年03月16日 | 図の出典を更新しました。 |
| 2014年10月03日 | 5年相対生存率データを更新しました。 |
| 2013年03月26日 | 内容を更新しました。 |
| 2013年02月14日 | 「内視鏡治療」の図を更新しました。 |
| 2012年11月27日 | 「治療に伴う合併症とその対策」を追加しました。 |
| 2012年11月27日 | 「手術(外科治療)」「腹腔鏡下胃切除」を更新しました。 |
| 2012年11月02日 | 「治療成績」を更新しました。 |
| 2012年10月29日 | 「内視鏡治療」「薬物療法(抗がん剤治療)」を更新しました。 |
| 2012年10月26日 | 更新履歴を追加しました。 |
| 2012年10月15日 | 内容を更新しました。 |
| 2012年06月22日 | 内容を更新しました。 |
| 2012年06月05日 | 内容を更新しました。タブ形式に変更しました。 |
| 2007年04月02日 | 掲載しました。 |
